生物等效性试验全面信息咨询指南
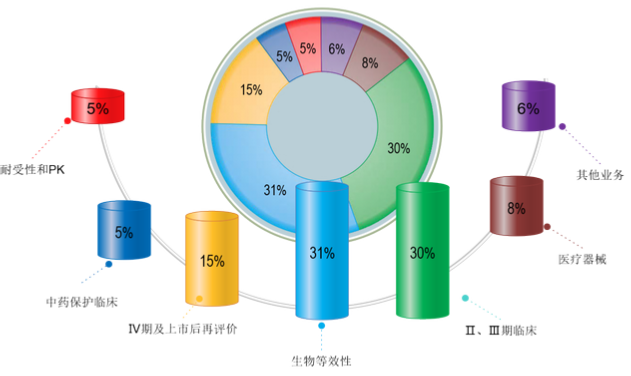
生物等效性试验是药物研发和注册过程中至关重要的环节,主要用于验证仿制药与原研药在生物体内吸收速度和程度的相似性。以下是对生物等效性试验的全面信息咨询内容:
一、生物等效性试验的基本概念
生物等效性试验是通过比较受试制剂(通常是仿制药)和参比制剂(原研药)在健康受试者体内的药代动力学参数,来评价两种制剂是否具有生物等效性。主要评价指标包括AUC(血药浓度-时间曲线下面积)和Cmax(峰值浓度)。
二、试验设计要求
- 试验设计通常采用随机、交叉、单剂量给药的设计方案
- 受试者选择:一般为18-45岁健康成年人
- 样本量计算需基于预试验数据或文献资料
- 清洗期的设置需考虑药物的半衰期
三、关键实施环节
- 伦理审查和知情同意:必须通过伦理委员会审批
- 生物样本采集:需制定详细的采样时间点方案
- 分析方法验证:生物样本分析方法必须经过完整验证
- 数据管理和统计分析:采用等效性检验方法
四、法规要求
- 必须遵循各国药品监管机构的相关指导原则
- 在中国需符合NMPA《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导原则》
- 在美国需符合FDA相关指导原则
五、常见问题与解决方案
- 个体变异大的问题:可通过增加样本量或采用重复设计解决
- 分析方法灵敏度不足:需优化检测方法
- 制剂处方工艺差异:需在试验前充分进行体外研究
六、咨询服务内容
专业的生物等效性试验咨询服务应包括:试验方案设计、伦理申报指导、CRO机构选择、数据分析支持和注册申报资料准备等全方位服务。
生物等效性试验的成功实施需要多学科团队的密切配合,包括临床药理学家、统计学家、临床医生和分析化学家等专业人士。建议在试验开始前充分咨询相关专家,确保试验设计的科学性和合规性。
如若转载,请注明出处:http://www.yuedutiandi.com/product/6.html
更新时间:2026-04-16 07:12:04